La Membrane Plasmique BORG
LA MEMBRANE PLASMIQUE
Préambule :
Nous sommes composés d’une mosaïque de cellules différentes, qui forme des organes. Tout commence par les cellules souches qui vont être capables de se diviser et se différencier. Toutes ces cellules sont différentes au microscope mais elles présentent des points communs, des propriétés cardinales qui les rassemblent. On peut observer leur forme et leur organisation.
La membrane plasmique permet de délimiter la cellule, d’isoler la cellule du monde extérieur ce qui peut éventuellement la protéger, mais aussi lui permet de communiquer avec l’extérieur grâce aux signaux solubles, protéines transmembranaires, etc… Elle joue un rôle de barrière et d’échange.
On va souvent prendre comme exemple les cellules épithéliales comme dans le tube digestif constitué de cellules très ordonnées qui permettent de lui donner sa forme mais aussi lui servent de système de défense (par exemple bactérienne) et d’échange (gestion des nutriments, eau…). Les cellules sont en cohésion les unes à côté des autres, elles ne sont donc pas isolées, et peuvent communiquer avec l’extérieur et entre elles. On peut donc penser qu’il existe un système de jonctions entre les cellules.
Ayant une forme de tube, le pôle apical des cellules est en contact avec la lumière du tube et donc les nutriments (et solutés aqueux). Alors le pôle basal des cellules est en contact avec la lame basale. Le noyau est plutôt basal. Il existe différents marqueurs selon le type de cellule.
Les propriétés biochimiques et fonctionnelles sont différentes selon la membrane latérale, basale et apicale.
Ch1 – Fig 1 : Schéma d’organisation d’une cellule eucaryote animale
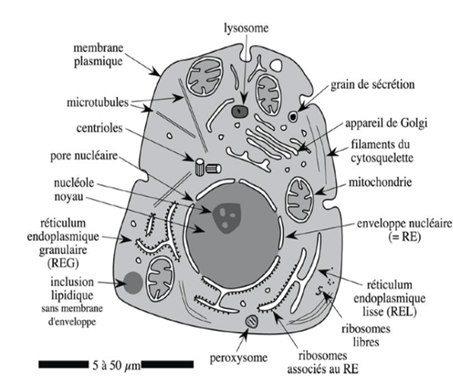
Il s’agit d’une cellule de l’épithélium intestinal dont la membrane a été marquée par immunocytochimie en faisant réagir des anticorps avec les protéines de la membrane. On peut ainsi observer que :
- La structure est bien définie
- La membrane est plus colorée d’un côté que de l’autre
à Il y a plus de protéines d’un côté
- La membrane représente une séparation entre les milieux extra/intercellulaires
à La membrane est impliquée dans la communication et l’échange
- On voit que la cellule intestinale est polarisée
- La cellule communique avec les autres cellules et avec l’extérieur
- Introduction : la membrane plamsique (MP)
La membrane plasmique est une enveloppe continue entre les milieux intra/extracellulaires. Elle délimite toute cellules (nous on va étudier les cellules eucaryotes). Elle sépare l’intérieur (cytosol) de l’extérieur.
Elle correspond à une frontière, une barrière c’est pourquoi elle participe : aux interactions entre la cellule et la matrice extracellulaire, à la signalisation (communication intercellulaire, elle réceptionne des signaux qui viennent de l’extérieur qui franchissent ou se fixent à la membrane plasmique, pour accomplir de fonctions) et aux échanges entre l’intérieur et l’extérieur de la cellule.
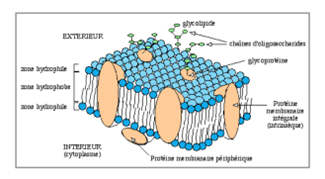
Elle présente 5 caractéristiques :
- C’est une bicouche lipidique
- Présence de glycoprotéines insérées dans membrane plasmique
- Elle est ASYMÉTRIQUE dans la composition de ses deux feuillets et dans les propriétés qui diffèrent entre le versant extracellulaire et le versant intracellulaire
- Elle est marquée par une certaine HÉTÉROGÉNÉITÉ entre les cellules et entre les domaines intra/extracellulaires…
- Elle entretient des relations avec le système endomembranaire, c’est-à-dire qu’elle n’est pas isolée des constituants intercellulaires.
Ch8 – Fig 1 : Les éléments constitutifs du système endomembranaire (échanges multiples et parfois complexes entre MP et SE (= ensemble de compartiments intracellulaires délimités par une membrane d’enveloppe équivalente de la MP)
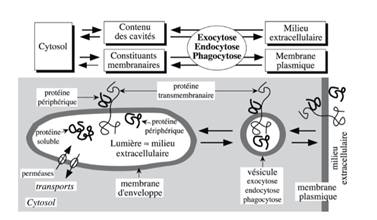
II. Composition de la membrane plasmique
- Les lipides (environ 50% du poids sec)
Les lipides présentent 2 extrémités :
- Un pôle hydrophile (qui aime l’eau) ou polaire
- Un pôle hydrophobe (qui n’aime pas l’eau) ou apolaire
Les lipides sont donc dits amphiphiles. L’amphiphilie est essentielle chez les lipides car elle leur permet de s’organiser en bicouche en milieu aqueux. (la tête sera automatiquement en contact avec l’eau).
Il y a 2 grandes catégories de lipides impliqués dans la membrane plasmique :
- Les phospholipides (1 groupement phosphate et 1 groupement lipidique)
- En majorité des phosphoglycérides, formés à partir d’une molécule de glycérol
- De la sphingomyéline, formée à partir de sphingosine
- Des dérivés de l’inositol (ex : glycosyl-phosphatidyl-inositol (GPI) un dérivé de l’inositol, qui a une structure particulière)
- Le cholestérol, dont la structure chimique est différente des phospholipides et qui est l’un des composants de structures participant à l’hétérogénéité de la membrane plasmique, les « radeaux lipidiques » = domaines qui ont des propriétés différentes (en composition et en fonction) du reste de la MP de la cellule. Les radeaux lipidiques sont riches en cholestérol, sphingosine et gangliosides.
Ch2 – Fig 1 : Phosphoglycéride (phosphatidylcholine) et sphingomyéline
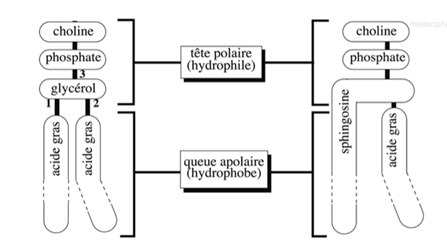
A gauche, on retrouve la phosphatidylcholine, constituée de :
- 1 molécule de choline, qui est un composé à fonction alcool (qui peut être remplacé par un autre)
- 1 molécule de glycérol (= alcool tri-esthérisée par un phosphate) à :
- 2 acides gras correspondant au pôle hydrophobe du lipide
- 1 groupement phosphate
A droite, la sphingomyéline est composée de (organisation générale conservée) :
- 1 molécule de choline
- 1 molécule de phosphate
- 1 acide aminé, la sphingosine, relié à un acide gras et remplaçant le glycérol
- Un des acides gras de la phosphatidylcholine
Il s’agit bien de structures différentes mais au sein desquelles on retrouve toujours une tête polaire et une queue apolaire. Elles ont donc les mêmes propriétés amphiphiles. Mis en solution aqueuse, les lipides (phospholipides) vont s’auto-assembler pour s’organiser en bicouche lipidique (double feuillet ou hémi-couche).
Les queues hydrophobes se mettent face à face.
- Les protéines (
50% du poids sec)
On distingue 3 classes de protéines membranaires :
- Les protéines intégrales (=qui traversent la MP) : Elles sont enchâssées dans la membrane et ne peuvent donc être extraites qu’avec des détergents ou des solvants organiques.
Elles peuvent être :
- Transmembranaires, elles ont alors un domaine extracellulaire et un domaine intracellulaire
- En épingles à cheveu, comme la cavéoline importante pour former les radeaux lipidiques, elle ne traverse pas totalement la MP mais elle est quand même considérée comme une protéine intégrale. Associées en permanence avec des acides gras.
- Les protéines ancrées à la membrane par des acides gras : Elles forment une association temporaire avec les acides gras. Il y a 2 catégories :
- Les protéines extracellulaires qui communiquent avec l’extérieur, ancrées par exemple avec le groupement GPI
- Les protéines cytosoliques, comme les protéines G.
- Les protéines périphériques situées sur le versant intracellulaire ou extracellulaire de la membrane.
- Si elles sont extracellulaires, elles peuvent être plus ou moins N-glycosylées. Elles ne sont pas directement fixées sur la MP, elles ont besoin d’un intermédiaire (protéine intégrale TMR ou ligand par exemple, synthèse REG + FMVP)
- Les protéines cytosoliques ne peuvent jamais être N-glycosylés. Elles ne sont pas directement fixées sur la membrane plasmique, mais ont besoin d’un intermédiaire.
Pour ces 3 catégories, les protéines cytosoliques (ou intracellulaires) sont synthétisées dans le cytosol alors que les autres le sont dans le REG. Ces dernières subissent des modifications telles que des N-glycosylations, sont transportées jusqu’à la membrane plasmique à travers un flux vectoriel permanent puis sont exposées dans le domaine extracellulaire.
Ch2 – Fig 2 : Les protéines de la membrane plasmique
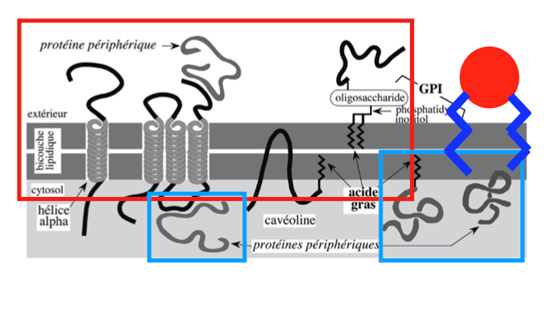
– Synthèse par le REG, flux membranaire vectoriel et permanent
– Synthèse par les ribosomes cytosoliques, ancrage temporaire
On peut identifier ici :
- Les protéines traversant la membrane, qui présentent des régions transmembranaires (parfois plusieurs régions transmembranaires pour une seule protéine) en hélice α. Ces zones sont composées d’environ 20 acides aminés hydrophobes (tyrosine, phénylalanine, isoleucine, avaline…) et ont des liaisons fortes avec les couches de lipides qui composent la membrane plasmique. La partie intracellulaire baigne dans le cytosol.
- Les protéines périphériques fixées à la membrane via des protéines intégrales transmembranaires.
- La cavéoline, qui est une protéine en épingle à cheveu. Elle traverse partiellement la membrane plasmique et est fixée en plus à la membrane plasmique avec un acide gras. Elle n’a pas de contact avec le milieu extracellulaire.
- Les protéines extracellulaires ancrées à la membrane plasmique grâce à un GPI. Celui-ci comporte une partie protéique, une partie sucrée et une partie lipidique.
- Les protéines périphériques au niveau intracellulaire, qui sont synthétisées dans le cytosol et associée de façon transitoire à la membrane plasmique. Elles sont très importantes dans le phénomène d’endocytose.
Ch4 – Fig 4 : Fixation d’une chaîne carbonée d’acides gras à une protéine cytosolique ou aux domaines cytosoliques d’une protéine avec domaines transmembranaires
La fixation d’une chaîne carbonée d’acides gras (acylation) à une protéine cytosolique lui permet de se fixer sur le versant cytosolique de la membrane.
Les protéines cytosoliques concernées peuvent être :
- Des protéines G (à gauche)
- Des cavéolines (à droite)
- Des NO-synthases (non représentées), qui sont des enzymes.
Ch4 – Fig 18 : Protéines spécifiques contrôlant les fonctions des protéines G
Les protéines G sont des oscillateurs (intérupteurs) moléculaires dont l’oscillation est contrôlée par plusieurs éléments, comme les protéines GAP. Ainsi, une protéine G présente :
- Une forme inactive quand elle est couplée au GDP et une forme active quand elle est couplée au GTP.
Elles ont une activité intrinsèque GTPase = elles vont naturellement hydrolyser le GDP en GTP.
Pour assurer leurs rôles, les protéines G sont nécessairement ancrées à la membrane via des acides gras. Active protéine Ras qui va à son tour entrainer la prolifération cellulaire.
- Les sucres (environ 5 et 10% du poids sec)
La présence de sucres a été mise en évidence par coloration spécifique ou par des lectines. Les lectines sont des composés produits par les végétaux qui peuvent fixer les sucres, et sont parfois couplées à des marqueurs fluorescents pour visualiser les sucres.
Les sucres ne sont JAMAIS LIBRES mais toujours liés à :
- Des protéines, ce sont les glycoprotéines
- Ou des lipides, formant les glycolipides.
Les sucres sont greffés aux lipides ou protéines au niveau du REG. Ils ne se trouvent que sur la FACE EXTRACELLULAIRE de la membrane (d’où l’asymétrie de la MP par ex). Il en existe plusieurs variétés avec donc des rôles variés :
- Avec charge électrique : par exemple, NANA (N-Acétyl Neuraminic Acid, ou acide cyalique) a une charge négative, il est impliqué dans les échanges hydrominéraux
- Retrouvés sur régions extracellulaires des molécules d’adhérence :
-> SAM (Substrat Adhésion Molecules) : intégrines (doivent être glycosylées) qui permettent de s’ancrer à la matrice extracellulaire.
-> CAM (Cell Adhesion Molecule) : cadherines permettent de rendre une cellule adhérente à sa cellule voisine
- Les glyco-sphingolipides : on les retrouve sur les antigènes des groupes sanguins à la surface des cellules (ils déterminent sur le globule les groupes sanguins)
- Les protéoglycanes : ce sont des composés avec une partie protéique et une partie sucrée, situés sur le versant extracellulaire de la membrane plasmique, en particulier sur la matrice extracellulaire et la lame basale.
- Glycocalyx, composante sucrée extracellulaire de la MP, essentiel dans communication cellulaire, protection, et médiation d’interactions cellulaires
III. Architecture fonctionnelle de la membrane plasmique Figure 3 à 18
Comment les lipides, protéines etc.. s’associent en bicouche pour donner une fonction à la membrane plasmique ?
- La membrane plasmique est dite fluide (non rigide) : Les molécules lipidiques ont une certaine élasticité.
- La bicouche lipidique, formée de deux couches, inclut des têtes hydrophiles (représentées en rouge) et des queues hydrophobes à l’intérieur, face à face.
- Les protéines intégrales présentes peuvent soit traverser totalement la membrane, soit s’insérer partiellement dans une couche de la bicouche.
- La structure de la membrane a été décrite comme une mosaïque fluide : éléments de composition différente (lipides, protéines) et fluide car au niveau moléculaire elle est en mouvement perpétuel.
- La membrane plasmique est asymétrique
L’asymétrie de la membrane plasmique est influencée par plusieurs éléments :
- La composition lipidique des 2 hémi-couches (feuillets) de la MP est différente.
- Les sucres (sous forme de glycoprotéines/glycolipides) sont seulement sur le versant extracellulaire.
- Les ponts disulfures (PDS) entre les résidus cystéine se forment uniquement sur le versant extracellulaires (milieu oxydant contrairement au milieu IC qui est réducteur) qui permettent le repliement de la protéine. Les protéines intracellulaires/TMR peuvent avoir des cystéines mais celles-ci ne feront pas de PDS.
- Les protéines périphériques cytosoliques d’association avec le cytosquelette sont en proportions différentes : hétérogénéité (clathrine : Seulement intracellulaire (impliquée dans endocytose et exocytose, + hétérogénéité des domaines membranaires (lipides+ protéines)).
EXEMPLE LES RADEAUX LIPIDIQUES
Concentrés de protéines peu présentes dans un endroit particulier de la MP (cavéoline, récepteurs, protéines ancrées via GPI, protéines G, NO- synthase, protéine couplée avec GTP) ➔ Ils ont une fonction importante de signalisation
Figure 4 : Cytosol:
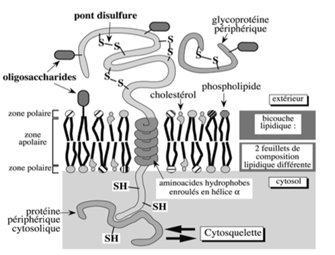
Les groupements sulfhydryles (-SH) des cystéines n’y forment pas de liaisons disulfure (S-S) à cause de l’environnement réducteur, qui empêche leur formation
Les groupements disulfures sont présents uniquement au niveau extracellulaire, ils vont aider les protéines à avoir une conformation spécifique pour leur fonction.
En extracellulaire, les protéines périphériques extracellulaires peuvent être glycosylées et former des ponts disulfures, et se fixer à des protéines intégrales. La présence de ponts disulfures dans cet espace oxydant favorise les conformations protéiques spécifiques à leur fonction.
La protéine transmembranaire vers le centre de la figure : oligosaccharides présents sur sa partie extracellulaire mais absents sur sa partie intracellulaire.
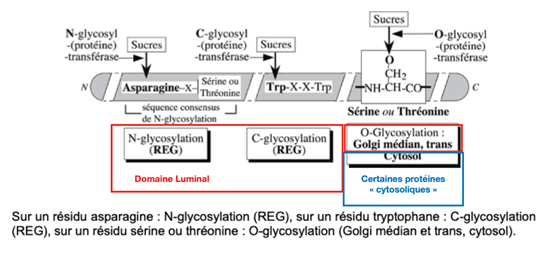
Voir plus loin : Figure 16 Chapitre 8 : Les 3 mécanismes de glycosylation des protéines :
RAPPEL : Les domaines cytosoliques des protéines transmembranaires ne sont jamais glycosylés
B) La membrane plasmique : mouvements des constituants à l’échelle moléculaire
La membrane plasmique est décrite comme une mosaïque fluide, car elle est constituée de nombreux composants lipidiques et protéiques (d’où l’image de la mosaïque) en mouvement (d’où la notion de fluidité).
Pour mettre ces mouvements en évidence, on étudie des mouvements sur des fantômes (ghost) on utilise des globules rouges dans un milieu hypotonique, on fait éclater les membranes et on étudie ces préparations de membranes. On peut utiliser les liposomes également.
1) Les lipides
Les lipides peuvent être animés par plusieurs types (3) de mouvements :
- La diffusion latérale au sein de la membrane
- La rotation sur place
- Le flip-flop (passage d’un lipide d’une hémicouche à une autre) qui demande de l’énergie d’une face de la membrane à une autre.
Ce mouvement est géré par des enzymes, les flippases
Il ne se fait pas que dans la membrane plasmique, mais aussi dans d’autres membranes de systèmes endomembranaires comme par exemple :
- Pour la N-glycosylation du dolichol (isoprénoïde) au niveau du REG
- La fabrication de l’ancre GPI au niveau du REG (la lumière du REG est équivalente au milieu extracellulaire) …
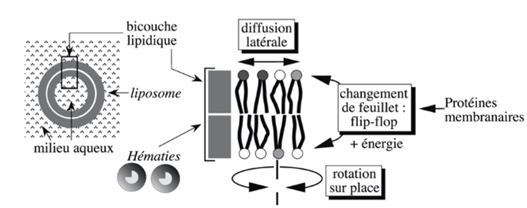
Ch2 – Fig 5 : Mouvements des lipides membranaires
Les liposomes sont des structures formées en laboratoire à partir de phospholipides. Ils sont utilisés en pharmaceutique car ils peuvent intégrer des substances dans leurs vésicules, ce qui permet de protéger les médicaments jusqu’à ce qu’ils aient atteint le lieu ciblé.
Lorsqu’on place ces liposomes en milieu aqueux, l’amphiphilie entraîne une organisation en bicouche.
Ces mouvements de lipides créent une fluidité de la membrane, qui dépend cependant de 3 paramètres :
- La température : une diminution de la température entraîne une rigidification de la membrane car il y a alors moins de mouvements des lipides
- La concentration de cholestérol : plus la concentration de cholestérol est importante, moins la membrane est fluide
- La nature des phospholipides : les lipides peuvent être saturés ou insaturés et plus il y a de lipides saturés, plus la membrane est rigide.
Par exemple, des bactéries vivant normalement à 37°C, placées dans un environnement à 4°C, subissent une rigidification de leur membrane. Pour pallier ce phénomène, elles produisent davantage de lipides insaturés.
Ch8 – Fig 1: Les éléments constitutifs du système endomembranaire
Les lipides et les protéines sont synthétisés et glycosylés dans le REG. Ils sont alors transportés du REG à la membrane plasmique au sein de vésicules, puis libérés par un phénomène d’exocytose.
2) Les protéines
Les protéines subissent 2 sortes de mouvements :
- La diffusion latérale dans le plan de la membrane
- La rotation
Pour les protéines, il n’existe pas de flip-flop, contrairement aux lipides, il y existe une limitation des mouvements des protéines (dynamisme distinct de celui des lipides)
Ch2 – Fig 6 : Mouvements des protéines membranaires dans le plan de la membrane, le phénomène de « capping » des lymphocytes
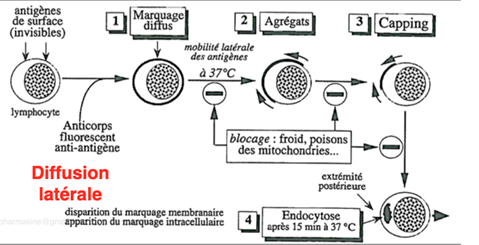
Les lymphocytes (vulgairement appelé « globule blanc ») sont des cellules du système immunitaire qui participent à la défense de facteurs pathogènes exogènes ou endogènes. Ils possèdent un noyau et une membrane plasmique.
On peut mettre les protéines de la membrane plasmique en évidence par la technique d’immunocytochimie en considérant ces protéines comme des antigènes que l’on met en présence d’anticorps couplés à un composé fluorescent. (fluochrome ou radioisotope)
- A 4°C, la fluorescence est diffuse au sein de la membrane. Les protéines sont réparties partout sur la membrane.
- A 37°C, on observe une polarisation de la fluorescence à un certain endroit de la membrane.
- Les protéines s’agrègent à un pôle de la cellule, qu’on appelle le capuchon ou le « cap » (d’où le terme du phénomène de « capping »).
Le phénomène de capping peut être bloqué par :
- Une diminution de T°, qui empêche le mouvement des protéines et rigidifie la membrane,
- Des poisons des mitochondries car cette réaction nécessite de l’énergie qui est puisée dans les mitochondries.
Après 15-20 minutes, la fluorescence se retrouve à l’intérieur de la cellule sous forme d’agrégats : il y a eu endocytose des protéines.
Si l’on poursuit encore l’expérience, la fluorescence disparaît car les antigènes ont été dégradés.
Ch2 – Fig 7 : Les 4 mécanismes limitant la diffusion latérale des protéines
La diffusion latérale des protéines peut être physiquement diminuée, voire empêchée par la présence de :
- Protéines membranaires ancrées dans le cytosquelette (leur mobilité est limitée par leur capacité à se fixer au cytosquelette = structure rigide qui fixe des protéines mb et les empêche de bouger)
- Protéines membranaires en interaction ferme avec la matrice extracellulaire, appelées SAM
- Protéines membranaires associées et interagissant entre elles (homotypique, hétérotypique),
- Protéines membranaires portées par 2 cellules voisines interagissant entre elles, ce sont les CAM, qui constituent souvent des jonctions cellulaires (comme les jonctions serrées).
C) La membrane plasmique : modification de sa composition chimique par disparition ou clivage enzymatique
Tout d’abord, la composition chimique de la membrane plasmique peut être modifiée par clivage. Celui-ci peut être réalisé par :
- Des protéases, qui sont des enzymes (protéines) capables de cliver d’autres protéines et agissant dans plusieurs domaines :
- Extracellulaire, comme la famille ADAM ou les MMP
- Intracellulaire ou cytosolique, comme la caspase
- Intramembranaire (sécrétase) ou transmembranaire
- Des phospholipases, qui sont des enzymes capables de cliver des lipides (en particulier des phospholipides) et agissant aussi dans plusieurs domaines :
- Extracellulaire, comme les GPI
- Cytosolique
- Intramembranaire, notamment lors de la formation d’IP3 et de DAG (seconds messagers) qui sont des moyens pour la cellule de communiquer de la membrane plasmique au cytosol (ils sont le fruit du découpage de phosphoinositide par des phospholipases).
Mais la membrane plasmique peut aussi voir sa composition chimique modifiée à la suite du détachement de protéines ancrées à la face cytosolique de la membrane plasmique (ex : protéines G associés acide gras, ils peuvent être dissociés si l’AG disparaît).
Ch2 – Fig 8 : Le clivage enzymatique des lipides et des protéines membranaires
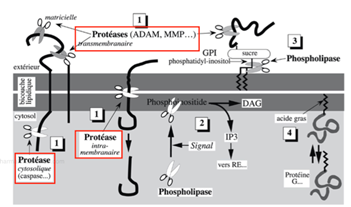
A gauche, une protéine intégrale avec une région transmembranaire est découpée :
- À 2 endroits par des protéases agissant dans le domaine extracellulaire
- À un endroit par une protéase cytosolique appelée caspase.
Certaines protéines peuvent être clivées au niveau transmembranaire, c’est-à-dire entre les deux couches lipidiques.
Une glycoprotéine associée à la membrane plasmique par un groupement GPI peut se voir clivée en 2 endroits :
- Dans sa partie protéique par une protéase,
- Dans sa partie lipidique par une phospholipase.
Certains phospholipides, les phosphoinositides, peuvent être clivés et ainsi libérer des messagers :
- Les DAG (diacylglycérol), qui restent dans la membrane plasmique
- L’IP3, qui se dirige vers les organites du cytosol tels que le réticulum endoplasmique.
A droite, un acide gras ancrant une particule protéique à la membrane plasmique peut se détacher de la membrane plasmique, tout en restant accrochée à la protéine. C’est le cas par exemple des protéines G.
EN RESUME
1. Protéases ExtraCellulaires (EC) :
– ADAM (A Disintegrin And Metalloproteinase) et MMP (Matrix MetalloProteinases) clivent les protéinestransmembranaires ou composants matricielsextracellulaires.
2. Protéases Cytosoliques :
– Caspases, impliquées dans l’apoptose
3. Protéases Intra-Membranaires :
– La sécrétase découpe la transmembranaire
4. Protéases Transmembranaires :
→ Rappel : Les petits fragments protéiques issus du clivage par ces enzymes EC ou IC peuvent se transformer en signaux.
Les « Ciseaux moléculaires » décrivent les enzymes clivant les composants de la membrane plasmique, essentiels à la signalisation et régulation cellulaire.
Ch11 – Fig 9 : Voie d’activation protéine G, phospholipase C, phosphositides
Dans la membrane plasmique, on trouve un récepteur particulier, nommé RCPG, qui est capable de recevoir un ligand, comme l’acétylcholine.
La fixation de ce ligand active la protéine G en entraînant son couplage avec un GTP.
La protéine G va ensuite activer une enzyme, la phospholipase.
Cette enzyme clivée alors un phosphoinosityl, aussi appelé PIP2, qui donne 2 messagers, DAG et IP3 :
- Le DAG reste dans la membrane et peut activer l’enzyme protéine-kinase C capable de modifier les protéines par phosphorylation
- L’IP3 va créer un signal dans des compartiments intracellulaires tels que l’appareil de Golgi, le réticulum endoplasmique… qui contiennent sur leurs membranes des récepteurs pour l’IP3.
- Ces organites libèrent alors du calcium dans le cytosol pour activer :
- D’autres enzymes kinases, à l’origine de phosphorylations
- La NO-synthase, à l’origine d’une production de monoxyde d’azote NO.
Le clivage permet donc d’organiser une signalisation à l’intérieur de la cellule qui part de la membrane vers le cytosol.
D) Les régions de la membrane plasmique font preuve d’une augmentation de la surface d’échange avec le milieu extracellulaire
La membrane plasmique peut se spécialiser dans le but d’accroître sa surface d’échange avec le milieu extérieur en faisant des expansions qui peuvent être de différents types :
- Microvillosités, qui sont des expansions cytoplasmiques en doigts de gants avec un cytosquelette d’actine.
- Colon
- Stéréocils, des expansions plus grandes que les microvillosités contenant des filaments d’actine
- Oreille interne
- Cils, c’est-à-dire des expansions cytoplasmiques à la membrane qui contiennent des microtubules et des protéines associées, et qui peuvent être mobiles ou non.
- Glomérule rénal : avec ses villosités, crée une structure cérébriforme. Rôle essentiel dans la filtration de l’urine primitive et l’élimination de l’eau et des sels minéraux. La structure ramifiée du glomérule augmente les capacités d’excrétion et de réabsorption de l’eau
- Replis du pôle basal des cellules épithéliales
- Le rein est un organe capable de filtrer de grandes quantités (éliminer les toxines de la circulation sanguine) d’urine et de récupérer beaucoup d’eau. Les cellules du rein ont donc besoin d’importantes surfaces d’échange, c’est pourquoi on observe des replis de la membrane plasmique du pôle basal des cellules épithéliales intervenant dans les échanges hydrominéraux.
Dans les membranes, on trouve des molécules de transport qui font transiter l’eau au sein de pores, ce sont les aquaporines (découvertes par Peter Agre, prix Nobel de chimie en 2003). On trouve aussi de nombreuses mitochondries car une telle absorption nécessite beaucoup d’énergie.
Mentionné mais pas expliqué par le prof
4 ROLES PRINCIPAUX DE LA MP
- Motilité cellulaire, c’est-à-dire la capacité qu’a une cellule à se mouvoir sur un substrat (Ch7)
- L’endocytose, l’exocytose et l’adhérence de la membrane plasmique sont nécessaires à cette motilité
- Communication intercellulaire (Ch11)
- Adhérence : les molécules d’adhérence sont des protéines membranaires spécialisées (SAM, CAM)
- 2 types de transports :
– Sans mouvements de la MP (passif avec ou san perméase)
– Avec mouvement de la MP (endo/exocytose et phagocytose)
IV. Adhérence intercellulaire ou adhérence entre la cellule et la MEC
- Généralités
Les molécules d’adhérence sont toutes des glycoprotéines, qui sont donc synthétisées dans le REG.
Il y en a 2 types :
- Les CAM (Cell Adhesion Molecule), qui permettent l’adhérence cellulaire
- Les SAM (Sustate Adhesion Molecule), dont le rôle est d’assurer l’adhérence à la matrice extracellulaire ou à la lame basale.
On distingue 4 principales superfamilles de molécules d’adhérence :
- Les Immunoglobulines (Ig), indépendante du calcium
- Les Cadhérines dépendantes du calcium
- Les Sélectines dépendantes du calcium
- Les Intégrines dépendantes du calcium
(Il en existe d’autres mais elles ne seront pas étudiées…)
Edelman (Nobel 1972) a découvert l’existence de molécules d’adhérence et a prouvé qu’on peut distinguer différentes familles parmi elles car il y a une spécificité de cette adhérence. Il a notamment identifié les NCAM (Ig) et les LCAN (cadhérines).
L’adhérence peut provoquer le rapprochement de 2 cellules, mais elle peut aussi être à l’origine de la répulsion entre 2 cellules.
Les molécules d’adhérence ont 2 caractéristiques :
- Adhérence AVEC/SANS calcium extracellulaire Leur capacité d’adhérence nécessite l’utilisation de Ca++ ou pas
- Présentes ou non dans la membrane plasmique, 4 catégories :Présentes et fonctionnelles d’emblée CAM IgCadhérinesPrésentes et à activer IntégrinesAbsentes mais disponibles par exocytose Sélectines transportées à la membrane plasmique sous l’effet d’un signal d’insertionAbsentes : elles ne sont pas exprimées normalement dans la cellule, mais sous l’effet d’un signal, le gène qui code pour cette protéine sera transcrit et traduit, ce qui nécessite davantage de temps.
Pour montrer expérimentalement la dépendance des molécules d’adhérence au calcium, on va tenter d’obtenir une suspension de cellules épithéliales dissociées à partir d’un fragment de tissu.
On les plonge dans un milieu de dissociation qui ne possède pas de calcium, et pourvu de chélateurs de calcium (dont le rôle est de séquestrer le calcium). Les cellules perdent alors leur capacité d’adhérence.
Si l’on ajoute des protéases, les cellules perdent en plus leur géométrie, elles deviennent rondes et ne peuvent plus adhérer entre elles.
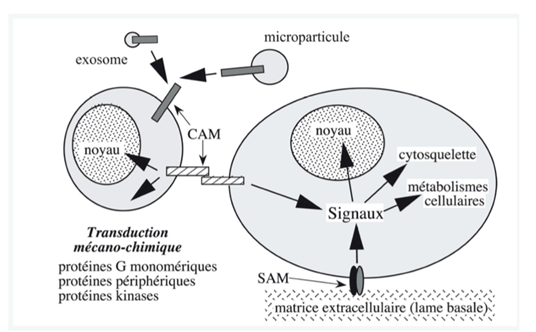
Ch2 – Fig 9 : Transduction mécano-chimique déclenchée par la mise en jeu des molécules d’adhérence SAM ou CAM
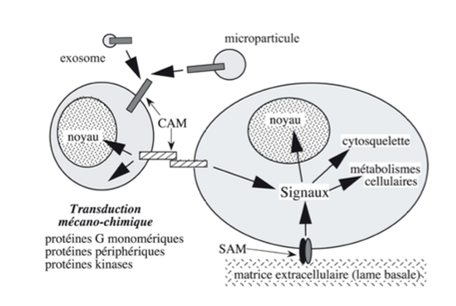
L’adhérence induit une transduction mécano-chimique : lorsqu’il y a adhérence entre 2 cellules, des signaux sont envoyés vers le noyau, le cytosquelette, les métabolismes cellulaires…
Ces signaux permettent une réorganisation de l’architecture cellulaire et du métabolisme cytosolique et nucléaire, via les protéines G, des enzymes (comme les kinases), des protéines périphériques cytosoliques…
Une anomalie de ces molécules d’adhérence ou un clivage enzymatique (assuré par exemple par une enzyme ADAM ou MMP) peut être à l’origine d’une augmentation de la mobilité cellulaire (cancer, métastase, développement embryonnaire…).
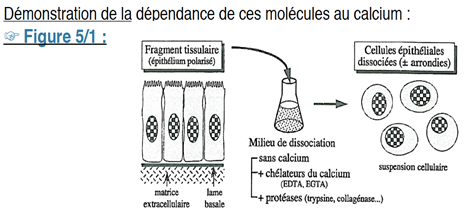
- B) Les CAM de la superfamille des Ig
Rappel : Toutes les molécules d’adhérence sont des glycoprotéines
NCAM (N : Neural : molécule trouvée au départ dans les neurones) : exprimée dans les neurones, mais aussi dans les muscles et dans plein d’autres cellules.
Elles ont un rôle d’adhérence mais peuvent aussi envoyer un signal dans la cellule (voir généralités…).
Leur adhérence est indépendante du Calcium (Ca++).
Superfamille très large
Les membres peuvent avoir un ou plusieurs domaines Ig, similaires à ceux trouvés dans les anticorps, avec un nombre variable de domaines selon les molécules. Cette famille inclut non seulement des molécules d’adhérence mais aussi d’autres types de molécules sur la surface cellulaire qui n’ont pas forcément des propriétés d’adhérence.
Pathologies
CAM L1 sontimpliquées dans
l’adhésion neurone-neurone et importantes pour le développement du SNC. NCAM, associée au cancer à petites cellules du poumon. CD4 est un récepteur pour le VIH.
Sur la partie extracellulaire, ces molécules présentent des boucles immunoglobulines stabilisées par ponts disulfures. Le nombre de domaine Ig est variable. Il permet une interaction directe avec d’autres molécules de la famille des Ig (rôle de CAM) mais aussi avec des molécules de la matrice (rôle de SAM)
Interaction
Il peut y avoir une interaction avec les molécules de la famille des intégrines à condition qu’il y ait du calcium dans le milieu. Elles peuvent être coupées par un certain nombre de protéases de la famille ADAM ou MMP. Au niveau intracellulaire, quand il y a liaison entre deux molécules il va y avoir une transduction du signal et des actions sur le cytosquelette notamment.
Ch2 – Fig 10 : Une molécule N-CAM
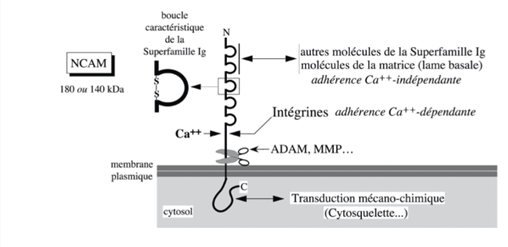
Une boucle Ig est faite avec un pont disulfure formé entre 2 résidus de cystéine.
Les intégrines se fixent de manière calcium dépendante à un domaine de la molécule NCAM proche de la membrane plasmique. Le domaine extracellulaire de NCAM peut être clivé par des prothèses extracellulaires ou membranaires et libérées dans le milieu extracellulaire.
- C) Les cadhérines, deuxième famille de CAM
Famille avec de nombreux membres, la plus connues est E-Cadhérine (initialement trouvée dans les cellules épithéliales). Les cadhérines se trouvent dans de nombreuses cellules, dont les cellules épithéliales (au niveau des jonctions). Leur adhérence est dépendante du calcium.
Ch2 – Fig 11 : Les CAM de la superfamille des cadhérines
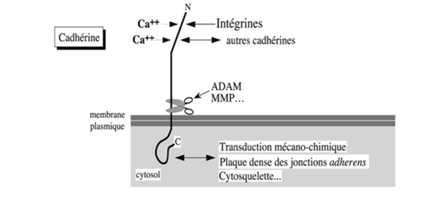
Il s’agit d’une glycoprotéine transmembranaire qui va soit interagir avecd’autres cadhérines soit avec d’autres molécules d’adhérence.
→ Transduction mécano-chimique et modulation du cytosquelette
Les cadhérines peuvent fixer 2 types de molécules :
- Des intégrines
- D’autres cadhérines de cellules voisines (au niveau de jonctions intercellulaires)
Dans tous les cas, l’adhérence se fait toujours en présence de calcium.
Les cadhérines interagissent de 2 façons différentes :
- Par leur domaine extracellulaire avec :
- Des intégrines
- D’autres cadhérines (« scratch »)
- Par leur domaine cytosolique avec :
- Certains constituants du cytosquelette (figure 13 ch 7)
- Les constituants de la « plaque dense » pour les jonctions intermédiaires, ou adhérentes aux pôles apicaux des cellules polarisées.
Mise en évidence : En utilisant des anticorps anti-(E)cadhérines couplées à des fluorochromes en immunocytochimie, on constate que les membranes en contact (ou membranes jonctionnelles) sont marquées.
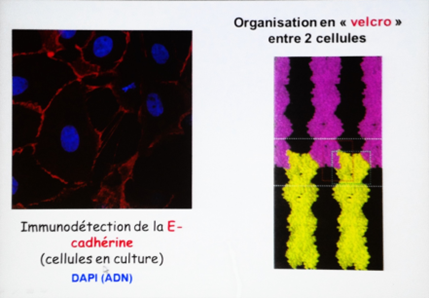
Ainsi, seules les membranes jonctionnelles contiennent des cadhérines (principalement).
Les cadhérines se retrouvent face à face et s’organisent en « velcro » pour permettre la cohésion entre 2 cellules (CAM).
Les cadhérines sont impliquées dans certaines pathologies :
- Les cancers : les cadhérines sont peu ou ne sont plus exprimées dans cellules tumorales, ce qui permet à ces dernières de quitter leur lieu initial et d’aller proliférer ailleurs à agressivité accrue dans les cancers
- L’inhibition de contact : pathologie cutanée auto-immune
D) Les sélectines : troisième famille de CAM
Les sélectines se situent dans les leucocytes, les plaquettes, et les cellules endothéliales.
Leur adhérence est calcium-dépendante.
Les sélectines s’insèrent à la membrane plasmique à la suite d’un signal extracellulaire (mécanique ou chimique), on parle de signal d’insertion.
Les sélectines jouent un rôle dans plusieurs pathologies comme le cancer, l’inflammation et elles servent de récepteurs à des agents pathogènes, notamment des bactéries (H.Pilori)
Ch2 – Fig 13 : Les sélectines
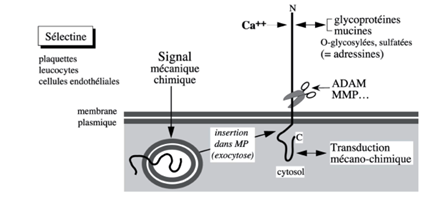
C’est un stimuli qui provoque l’insertion des sélectines dans la membrane plasmique par un phénomène d’exocytose (elles ne sont donc pas constitutives).
Sur ce type de récepteur peuvent, par la suite, se fixer à des adressines (glycoprotéine + mucine)
Elles peuvent être clivées par ADAMs ou MMP. Leur interaction avec des glycoprotéines de l’environnement contribue à la transduction mécano chimique.
Les sélectines jouent un rôle dans plusieurs pathologies comme le cancer, l’inflammation et elles servent de récepteurs à des agents pathogènes, notamment des bactéries (H.Pilori)
E) Les intégrines : rôle de CAM et de SAM
Comme SAM, les intégrines permettent l’adhérence aux molécules de la matrice extracellulaire et la lame basale, (en se fixant sur des protéines comme la fibronectine)
Comme CAM, les intégrines peuvent adhérer à des molécules de la superfamille des
Immunoglobulines (Ig) mais adhérence dépendante du calcium. Elles sont présentes dans de très nombreux types cellulaires (fibroblastes, cellules épithéliales,leucocytes, plaquettes…) selon la cellule on aura des intégrines différentes
Intégrines et pathologies
- Cancer (elles sont hyperactives)
- Maladies congénitales → intégrines altérées
- Récepteurs pour agents pathogènes : virus, bactéries
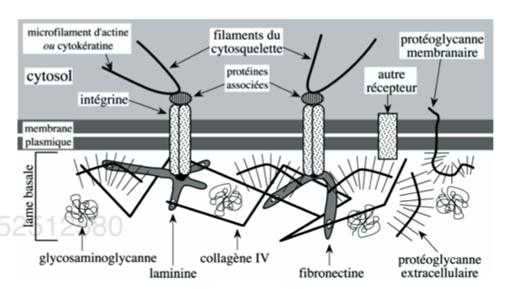
Ch2 – Fig 14 : Les intégrines
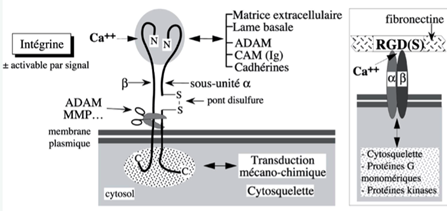
On remarque
- La présence de Calcium indispensable.
- Elles sont présentes sous forme de 2 chaines (2 sous unités) = glycoprotéines : α et β Il existe une quinzaine de sous unités alpha et 3 sous unités β qui peuvent se combiner entre- elles : donc grande diversité des intégristes.
- Elles peuvent interagir avec les protéines de la matrice et plus particulièrement celles de la lame basale (rôle de SAM), en particulier la fibronectine. Cette dernière a dans sa séquence protéique une séquence RGD(S) qui est la séquence d’interaction avec les intégrines.
- Elles peuvent aussi interagir avec d’autres protéines comme les cadhérines et les ADAMs (rôle de CAM).
- L’interaction de ces intégrines avec des molécules de la matrice ou des molécules adhérantes de cellules adjacentes va entrainer là encore des signaux et participer à la transduction mécanochimique.
- Elles permettent de relier les molécules de la matrice avec les molécules du cytosquelette. Ces interactions sont importantes pour permettre la polarisation des cellules.
Elles jouent donc le rôle de récepteurs cellulaires mais l’information va à la fois de l’extérieur de la cellule vers l’intérieur de la cellule et inversement.
F) Les jonctions intercellulaires : domaines de membrane spécialisés pour l’adhérence intercellulaire ou avec la matrice extracellulaire
1) Caractéristiques des jonctions intercellulaires
Les jonctions intercellulaires ont 4 caractéristiques :
- On les retrouve dans toutes les cellules (épithéliales ou non)
- Elles contiennent des CAM à domaine extracellulaire long ou court
- Elles constituent un domaine d’interaction entre membrane plasmique et cytosquelette
- Elles forment aussi un domaine de transduction mécano-chimique (kinases, protéines G…).
Ch2 – Fig 9 : La transduction mécano-chimique déclenchée par la mise en jeu des molécules d’adhérence CAM ou SAM
2) Critères pour classer les jonctions intercellulaires
On utilise 2 critères afin de classer les différentes jonctions :
- La morphologie – 3 types
- Bande complète ou zonula (occludens ou adherens) ceinture la cellule plutôt vers le pôle apical, plaques denses aux électrons au ME.
- Tâches ou macula
- Entre 2 cellules adjacentes : desmosomes ou jonctions communicantes = jonctions gap
- Entre cellule et lame basale : hémidesmosome
- Bande incomplète ou fascia
- La largeur de l’espace extracellulaire (intercellulaire), qui est déterminée par la composition des molécules d’adhérence :
- Espace large :
- CAM à long domaine extracellulaire
- Protéines périphériques spécialisées d’interaction avec le cytosquelette formant une « plaque »
- Espace étroit :
- CAM à court domaine extracellulaire (4 domaines transmembranaires)
- CAM à long domaine extracellulaire (au bord de la jonction)
- Protéines périphériques non organisées en plaque.
- Espace large :
Ch2 – Fig 15 : 3 types morphologiques de jonctions intercellulaires dans une cellule épithéliale polarisée
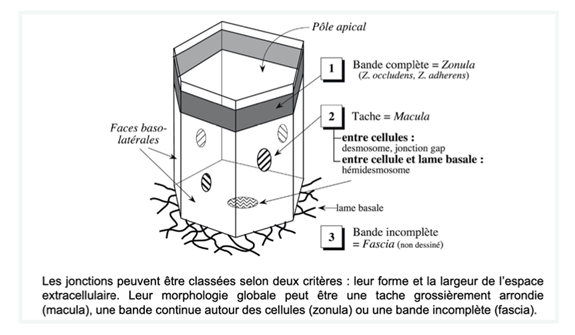
Ch2 – Fig 16 : Les 2 types de jonctions intercellulaires : la largeur de l’espace intercellulaire dépend de la nature des protéines membranaires de la jonction
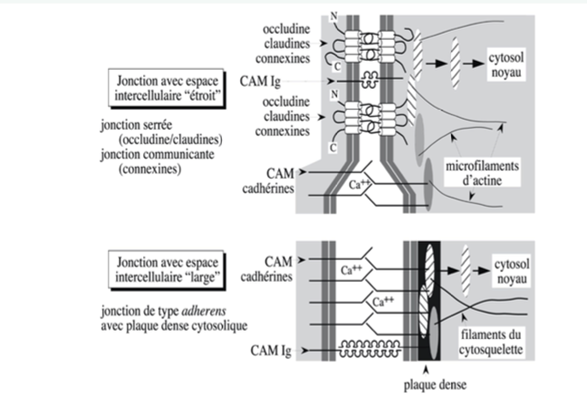
Au niveau d’une jonction avec un espace intercellulaire étroit, on retrouve 2 types : (la largeur de l’espace intercellulaire dépend de la nature des protéines membranaires de la jonction)
- Des occludines/claudines dans une jonction serrée
- Des connexines dans une jonction communicante.
Au niveau d’une jonction avec un espace intercellulaire large, il y a des CAM cadhérines et des Ig.
C’est le cas des jonctions adhérentes, qui sont composées :
- D’une plaque dense cytosolique
- De filaments du cytosquelette, c’est-à-dire des microfilaments d’actine ou des filaments intermédiaires.
3) Différents types de jonctions intercellulaires
Il existe 5 sortes de jonctions intercellulaires :
| Jonction serrée = Tight junction = Zonula occludens (ZO)Jonction communicante = Gap junction | Espace intercellulaire étroit (pas de plaque dense) |
| Jonction intermédiaire = Zonula adherens (ZA)Desmosome = Macula adherensHémi-desmosome | Espace intercellulaire large (complexe de jonction) |
Sur une cellule épithéliale polarisée, on observe des complexes de jonctions formés :
- De jonctions serrées
- De jonctions intermédiaires
- Parfois de desmosomes.
G) Jonction serrée
Caractéristique des cellules épithéliales
Caractéristiques :
- Bande continue,
- Espace intercellulaire étroit,
- CAM à 4 domaines transmembranaires : claudines, occludines
- CAM à domaine extracellulaire long : CAM Ig, cadhérines (en périphérie),
- Les jonctions serrées forment des radeaux lipidiques,
- Des protéines associées cytosoliques sont spécifiques aux jonctions serrées : ZO1, protéines G…
Dans une cellule épithéliale polarisée :
- Les jonctions serrées se situent à la frontière pôle apical-face basolatérale
- Elles permettent l’étanchéité relative, contrôlée par l’épithélium car le nombre de protéines claudines définit l’épaisseur de la membrane, ce qui impact sur l’étanchéité (plus la membrane est épaisse, plus elle est étanche).
Pathologies (dans les épithéliums polarisés) :
- Mutation des claudines à l’origine par exemple de troubles de l’audition
- Action de pathogènes (toxines bactériennes, virus…) conduisant à une perte d’étanchéité absolue de la couche épithéliale.
Claudine + occludine = étanchéité relative
Ch2 – Fig 17 : Jonction serrée (zonula occludens)
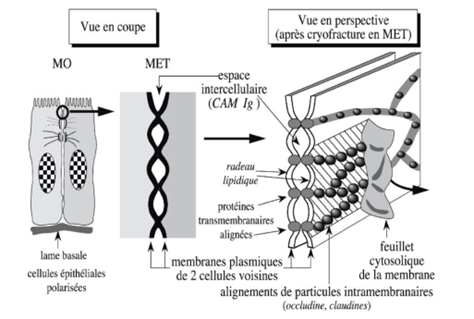
MO : Microscopie Optique / MET : Microscopie Électronique en Transmission
CAM : Cell Adhesion Molecule
JAM : Junctionnal Adhesion Molecule
La jonction serrée ou zonula occludens est caractéristique de la cellule épithéliale polarisée. Elle constitue une bande continue ceinturant la partie haute de la face latérale de la cellule à proximité du pôle apical. La jonction serrée est l’un des exemples de jonction à espace intercellulaire étroit point elle comprend 2 types de molécules d’adhérence : les CAM à 4 domaines trans cellulaire et à domaine extracellulaire court (occludine, claudines) et des CAM à domaine extracellulaire nom de la super-famille des Ig (dont les JAM), et de la superfamille des cadhérines.
On remarque que les jonctions serrées présentent de nombreux points de contact entre les membranes plasmiques des cellules voisines. Entre ces points de contact on trouve des radeaux lipidiques et des protéines transmembranaires (Ig CAM)
Ch2 – Fig 18 : Les alignements de claudine(s) ménagent des pores aqueux permettant les transports paracellulaires au travers de la jonction serrée
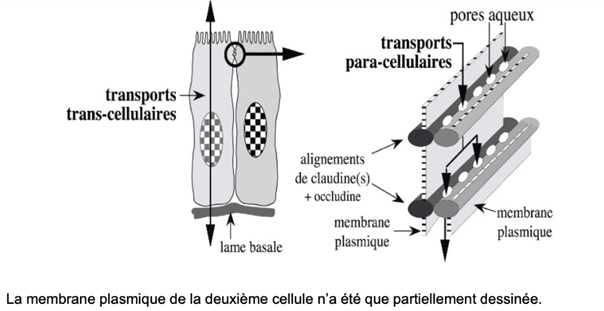
La présence de claudines est déterminante dans l’étanchéité.
Il peut y avoir un passage de composés à travers les pores aqueux organisés par les claudines, on parle alors de transport paracellulaire.
FONCTION
Barrière
Les jonctions serrées agissent comme une barrière relative, contrôlant le passage de l’eau et des substances dissoutes entre deux cellules épithéliales voisines.
→ Les alignements de claudines créent des pores aqueux pour le transport paracellulaire à travers la jonction serrée
→ Permet à des fluides de passer entre les cellules, (imperméabilité conservée mais possibilité de faire passer des molécules).
La présence des claudines au niveau de ces jonctions serrées est donc l’élément déterminant pour l’étanchéité et le transport paracellulaire (entre deux cellules, PAS DE DROITE À GAUCHE).
Transport
Le transport peut se faire de plusieurs manières :
– Paracellulaire qui se fait plus ou moins bien suivant la quantité de claudines.
– Transcellulaire, de haut en bas d’une seule et même cellule. Ce transport se fait plus facilement sans passer par les jonctions
H) Jonction communicante – gap junction (macula)
Caractéristiques :
- Forme arrondie (macula)
- Espace intercellulaire étroit
- CAM à 4 domaines transmembranaires : 6 connexines (en hexamère) forment 1 connexon (« canal »)
- CAM à domaine extracellulaire long : CAM Ig, cadhérines
- Protéines associées cytosoliques : protéines G…
- Les jonctions communicantes assurent le transport de cytosol à cytosol de petites molécules, ions (PM≤1000Da)
Les jonctions communicantes sont donc impliquées dans la communication intercellulaire, et la cellule peut contrôler leur nombre et leur perméabilité en régulant le nombre et l’ouverture de ces connexions.
Dans une cellule épithéliale polarisée, les jonctions communicantes sont situées sur la face basolatérale.
Dans les neurones et les astrocytes, elles permettent la formation de synapses électriques.
Pathologies
Les mutations de connexines, pouvant notamment entraîner une cataracte, sont impliqués dans cancers et maladies cardiaques.
Ch2 – Fig 20 : Jonction communicante
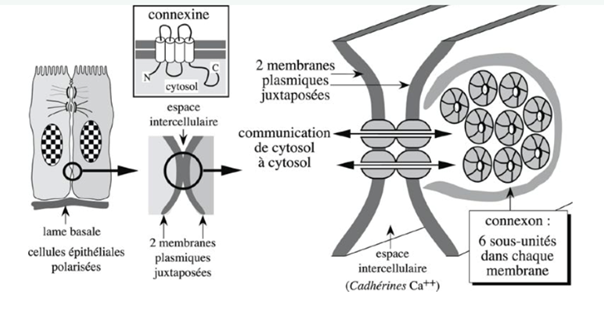
Structure
Les connexines sont des molécules transmembranaires avec quatre hélices alpha transmembranaires et des domaines extracellulaires courts.
Un connexon se forme avec 6 connexines, entre des cellules situées face à face, ce qui permet à certaines molécules de passer d’une cellule à l’autre.
Elles nécessitent du calcium pour leur fonction d’adhérence. À la périphérie de ces connexines on retrouve des molécules de la superfamille des Ig et des cadhérines. Les connexons sont régulés par le calcium, qui joue un rôle dans leur ouverture et fermeture : en présence de calcium, les canaux se ferment. Ce sont les boucles extracellulaires courtes des connexions qui assurent une adhérence calcium dépendante des cellules de contact.
Des CAM (cadhérines, CAM Ig) sont aussi présentes à la périphérie du domaine jonctionnel.
Rôle
Ces connexions jouent un rôle dans le passage de petites molécules, d’ion…(PM < 1000 Da = 1kDa) de cytosol à cytosol, ainsi elles permettent :
- Le couplage métabolique avec le passage d’ATP, IP3, peptides
- La communication intercellulaire nombre de ses jonctions et de leur perméabilité peuvent être contrôlés entre les cellules
Ch2 – Fig 22 : Les 3 directions des échanges métaboliques au travers d’un épithélium polarisé
Le transport de molécules par une jonction communicante répond à un signal.
Le transport transcellulaire s’effectue de haut en bas (du pôle apical au pôle basal), et participe à la communication intercellulaire.
I) Jonction intermédiaire – jonctions adhérens – zonula adhérences
Caractéristiques :
- Bande inconstante
- Espace intercellulaire large
- Les jonctions intermédiaires sont situées sur la face latérale des cellules, sous les jonctions serrées
- CAM à domaine extracellulaire long : CAM Ig, cadhérines
- Protéines spécialisées associées cytosoliques formant une « plaque » qui permet insertion de microfilaments d’actine
- Protéines G
- Les jonctions intermédiaires jouent un rôle dans la fermeture du tube neural au cours du développement embryonnaire.
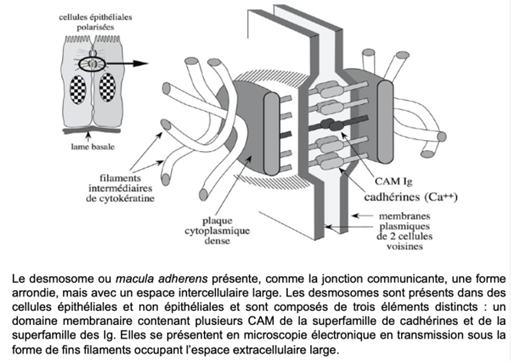
J) Desmosome – macula adherens
Caractéristiques :
- Forme arrondie
- Espace intercellulaire large
- CAM à domaine extracellulaire long : CAM Ig, cadhérines
- Protéines spécialisées associées cytosoliques formant une « plaque » qui permet l’insertion de filaments intermédiaires de :
- cytokératine (cellules épithéliales)
- cytokératine et vimentine (cellules épithéliales d’origine mésoblastique)
- Desmine (cardiomyocytes.)
- Protéines G
Elles permettent 2 choses importantes : servent de rivet au niveau des jonctions intercellulaires et servent au maintien de la forme des cellules on peut les comparer à des boutons de pression
K) Hémidesmosome
Caractéristiques :
- Les hémidesmosomes se concentrent au contact de la lame ou membrane basale, tandis que les desmosomes se trouvent sur la face latérale
- Les molécules d’adhérence des hémidesmosomes sont des intégrines capables d’ancrer la cellule avec du calcium en la fixant à des molécules de la matrice extracellulaire (fibronectine) alors que les desmosomes contiennent des cadhérines et des CAM Ig.
- Frome arrondie
Des filaments intermédiaires de cytokératine sont ici reliés à la plaque cytoplasmique dense qui borde l’espace intercellulaire, et d’où partent les cadhérines et les CAM Ig.
L’elimination des
Ch2 – Fig 24 : Les desmosomes des cellules épithéliales polarisées sont reliés entre eux par les filaments intermédiaires de cytokératine
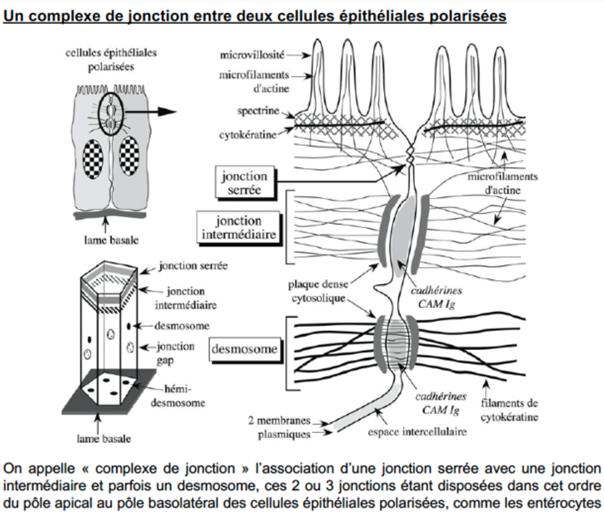
L’élimination des desmosomes ou hémidesmosome entrainerai la perte de l’architecture de la cellule ce qui peut conduire à son effondrement.
L) Transports sans mouvement de la membrane plasmique
Ch2 – Fig 25 : Les transports membranaires sans mouvement de la membrane plasmique
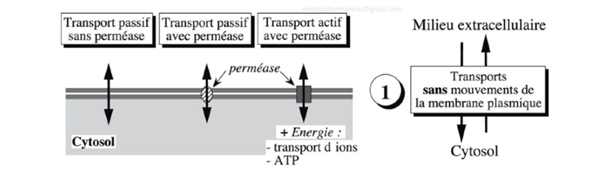
Le transport sans mouvement n’est pas observable au microscope puisque la membrane plasmique reste immobile, tout se passe à l’échelle moléculaire. Les éléments passent donc directement du milieu extracellulaire au cytosol en traversant la membrane plasmique.
Ni le système endomembranaire ni le cytosquelette n’interviennent au cours de ce type de mouvement.
On distingue 3 transports sans mouvement de la membrane plasmique possibles :
- Passif sans perméaseAucun besoin Phénomène de diffusion
- Passif avec perméasePas d’énergieL’enzyme creuse un canal dans la membrane plasmique
- Actif avec perméaseBesoin d’énergie, apportée par le transfert d’ions ou l’ATP
Rappel
Perméase = protéine intégrale enchâssée dans la MP qui va pouvoir faire canaux….
La MP est étanche, rien ne peut y passer de façon anarchique.
Ch2 – Fig 26 : Les différents modes de transports transmembranaire sans mouvement de la membrane plasmique
Au cours du transport passif sans perméase, certaines molécules (O2, CO2, éthanol, NO) sont capables de diffuser librement à travers la membrane plasmique du milieu le plus concentré vers le moins concentré selon le gradient de concentration.
Au cours du transport passif avec perméase, une ou plusieurs enzyme(s) crée(nt) un « canal » pour faire passer les composés du milieu le plus concentré au moins concentré (direction = gradient de concentration).
Il y a plusieurs types de transports passifs avec perméase :
- Les canaux ioniques ligand-dépendants (protéine G, GMPc, ATP, Ca2+), où un ligand ordonne l’ouverture ou la fermeture du canal
- Les canaux ioniques potentiel-dépendants (K+, Na+, Ca2+)
- Les transporteurs de glucose, d’acides aminés…
- Les aquaporines (pour l’eau, toujours de façon régulé)
Au cours du transport actif avec perméase, l’ATP peut être hydrolysé en ADP au niveau de la perméase, ce qui permet de récupérer l’énergie nécessaire au transport. C’est le cas :
- De la Na+/K+ ATPase qui fait expulser 3 ions sodium et fait entrer 2 ions potassium dans la cellule. Ces deux mouvements se font en même temps. Cette pompe peut être bloqué par une molécule : la Digoxine
- Des perméases ABC « détoxiquent » le cytosol de la cellule les produits toxiques naturels ou non (élimination de médicaments, etc..)
Par ailleurs, l’énergie peut provenir d’un transport d’ions (souvent de sodium). En effet, en traversant le canal du milieu le plus concentré vers le moins concentré, le sodium crée de l’énergie qui va permettre le transport d’un autre composant :
- Soit dans la même direction, c’est un symport (comme pour le glucose et le sodium)
- Soit dans l’autre sens, on parle d’antiport (avec par exemple les ions H+).
Le transport des ions au travers de la membrane plasmique a plusieurs conséquences (laissé pour la comprehension)
- Le maintien d’un gradient de concentration entre le cytosol et le milieu extracellulaire
- K+ très largement supérieur dans la cellule
- Na+ bien plus abondant dans le milieu extracellulaire
- Ca++ plus concentré dans le milieu extracellulaire
- Le gradient et l’activité de la Na+/K+ ATPase qui permet à la fois :
- Le transport d’ions
- Le potentiel de membrane qui est un potentiel de repos de -70mV.
V- Transports avec mouvements de la MP, pour les macromolécules
L’endocytose correspond à l’« entrée » dans la cellule, c’est-à-dire à l’internalisation de composés.
La phagocytose est un cas particulier d’endocytose.
L’exocytose consiste en une « sortie » de la cellule, autrement dit à l’expulsion des composés synthétisés ou des composants qui vont permettre à la cellule de renouveler sa membrane plasmique.
De tels transports nécessitent de l‘énergie et donc une contribution du cytosquelette.
De plus, il existe une balance endocytose/exocytose pour équilibrer ces phénomènes contraires.
Ch2 – Fig 27 : Les transports membranaires avec mouvements de la membrane plasmique
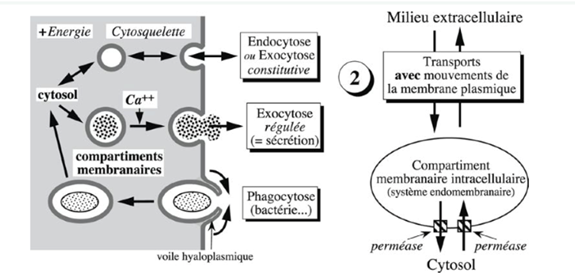
Les transports membranaires avec mouvements de la membrane sont observables au microscope.
Ils impliquent un compartiment membranaire intracellulaire, donc le système endomembranaire participe.
Ils nécessitent la formation temporaire de vésicules ou de vacuoles entourées par une membrane et permettent le transport de macromolécules voire d’organismes entiers comme des bactéries.
Les vacuoles ou vésicules permettent ainsi de véhiculer les composants dirigés dans une partie du cytosol. Le cytosol est à l’origine d’une partie du matériel transporté ou bien de sa destination finale. En raison de l’intervention du cytosquelette, ces transports nécessitent de l’énergie.
- Endocytose
Ch2 – Fig 28 : Les 5 types d’endocytose
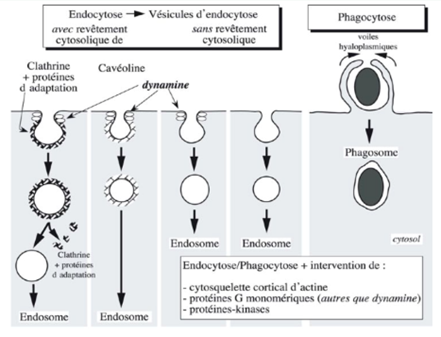
Au cours de l’endocytose, il y a toujours formation d’une invagination à la membrane plasmique sauf pour la phagocytose où l’élément à phagocyter est engouffré par des prolongements cytoplasmiques.
On utilise 3 critères de classification des endocytoses :
- La présence ou non d’un revêtement sur la face cytosolique des vésicules d’endocytose
- La nature et le volume des éléments du milieu extracellulaire internalisés
- L’intervention ou non d’une protéine G monomérique, la dynamine qui permet, sous l’effet de l’hydrolyse du GTP, de détacher la vésicule de la membrane.
On distingue ainsi 5 types d’endocytose :
- Vésicules bordées de clathrine et de protéines d’adaptation, qui seront dénudées, avec de la dynamine
- Vésicules bordées de cavéoline, non dénudées, avec de la dynamine
- Vésicules nues avec de la dynamine
- Vésicules nues sans dynamine
- Phagocytose, au cours de laquelle l’élément est englobé par des voiles hyaloplasmiques puis introduit dans le cytosol.
L’endocytose peut se faire de 3 façons :
- Via des vésicules recouvertes de clathrine (la clathrine est sous forme de tryskélion, c’est-à-dire de 3 chaînes lourdes et légères, cf schéma). C’est le cas des LDL et de leurs récepteurs. Les LDL sont des structures nécessaires au transport du cholestérol dans la circulation sanguine. En effet, le cholestérol est apporté par l’alimentation puis complexé en LDL dans le foie.
Rappel : un LDL est composé :
- De cholestérolDe phospholipidesDe protéines appelées apolipoprotéines, jouant le rôle de ligand du récepteur des LDL.
Ces particules LDL peuvent être capturées par les récepteurs aux LDL présents sur la membrane cellulaire, un processus qui nécessite la présence de clathrine et de protéines d’adaptation.
- Via des vésicules avec de la cavéoline
Dans ce cas, le déshabillage des vésicules n’est pas indispensable au transport cytosolique.
- Phagocytose
- Elle apparaît au niveau physiologique pour éliminer les éléments pathogènes étrangers à l’organisme (bactéries, billes de latex…).
- Lors de la phagocytose, plutôt que de s’invaginer vers l’intérieur, la membrane cellulaire s’étend pour englober la vésicule à l’aide de structures appelées voiles hyaloplasmiques, conduisant à l’internalisation de la vésicule.
- Le but de la phagocytose est d’utiliser les molécules énergétiques contenues dans les bactéries et autres éléments phagocytés pour assurer la nutrition de la cellule
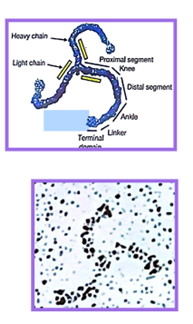
Ch2 – Fig 29 : Une molécule de LDL, agrégat de phospholipides, d’une protéine ligand du récepteur des LDL et de cholestérol
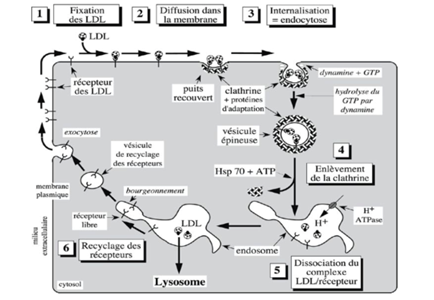
Hsp : Protéine de choc thermique
EXPLICATION DETAILLEE DU SCHEMA
Lorsqu’une cellule absorbe des substances, la vésicule formée par la membrane cellulaire est initialement recouverte de clathrine et des protéines spéciales qui facilitent ce processus.
Son revêtement de clathrine est ensuite retiré avant que la vésicule ne fusionne avec un endosome, une sorte de compartiment de traitement à l’intérieur de la cellule. L’hydrolyse du GTP pour détacher la vésicule de la membrane cellulaire.
Durant l’endocytose médiée par des récepteurs spécifiques, il peut se former deux principaux types de vésicules : celles recouvertes de cavéoline et celles recouvertes de clathrine.
La dynamine est requise pour former les vésicules recouvertes de clathrine. La clathrine est ensuite retirée avec l’aide d’une protéine chaperonne connue sous le nom de Hsp 70.
L’endocytose est primordiale pour utiliser les LDL. Si on bloque la dynamine on ne peut plus endocyter des LDL
Les cellules forment des vésicules de transport contenant les récepteurs aux LDL, qui permettent de récupérer et de recycler les récepteurs après qu’ils ont été utilisés pour introduire le cholestérol dans la cellule.
Les endosomes, caractérisés par un pH acide, facilitent le transport de protons dans différents compartiments cellulaires via des pompes à protons. Leur acidité provoque la dissociation des LDL de leurs récepteurs, permettant ainsi la possibilité de réutiliser ces récepteurs à travers le processus d’exocytose.
La HSP 70 (Heat Shock Protein), est responsable de la dissociation de la clathrine des endosomes, un processus qui requiert de l’ATP.
L’endocytose est primordiale pour utiliser les LDL. Si on bloque la dynamine on ne peut plus endocyter des LDL
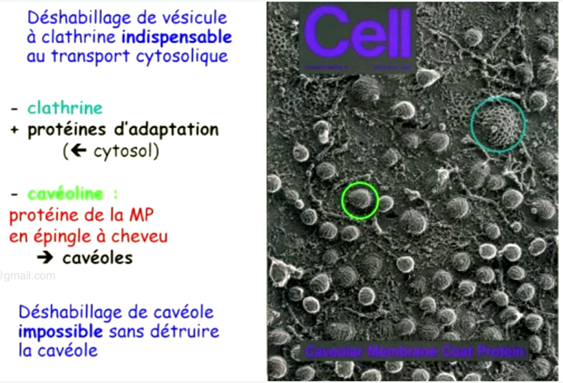
Ch2 – Fig 31 : L’endocytose par l’intermédiaire de récepteurs membranaires dans une cavéole
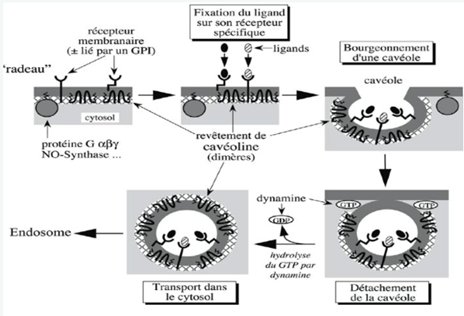
- Déshabillage des véhicules à la clathrine indispensable aux transports cytosolique
- Déshabillage de la cavéoline impossible sans destruction de la calvéole
- La dynamine détache la vésicule quand elle est quasiment formée
A noter : cavéoline ne se déshabille pas car détruirait la vésicule
Quant au devenir des substances captées par l’endocytose ou la phagocytose : le but principal est de fournir des nutriments à la cellule comme le cholestérol ou d’autres molécules phagocytées ce processus est conçu pour être sans perte toute la matière dégradée et récupérée du phagosome avant que celle-ci ne soit éliminé.
Le matériel endocyté ou phagocyté peut se diriger vers :
- L’appareil de Golgi, puis le réticulum endoplasmique et enfin le cytosolUn lysosomeLe cytosol, après traverser de la membrane d’enveloppe des endosomes et lysosomal au travers de perméases ou après effractionLa membrane plasmique par exocytose
Ch2 – Fig 32 : Phagocytose d’une bactérie par un macrophage ou un polynucléaire neutrophile
Des récepteurs, qui peuvent être des molécules d’adhérence, permettent de fixer la bactérie sur la membrane du macrophage ou du polynucléaire neutrophile.
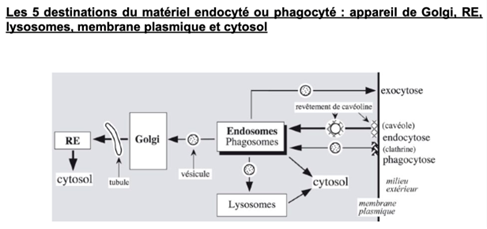
Ch2 – Fig 33 : Les 5 destinations du matériel endocyté ou phagocyté
Le matériel endocyté ou phagocyté peut se diriger vers :
- L’appareil de Golgi, puis le réticulum endoplasmique et enfin le cytosol
- Un lysosome
- Le cytosol
- La membrane plasmique par exocytose
B) Exocytose
Ch2 – Fig 27 : Les transports membranaires avec mouvements de la membrane plasmique
Il existe 2 types d’exocytose :
- L’exocytose constitutive : C’est un échange permanent entre la membrane plasmique et le milieu extracellulaire
- L’exocytose régulée ou provoquée
- Elle est déclenchée sous effet d’un signal, on parle aussi de sécrétion
- C’est le cas de l’exocytose d’insuline stockée dans le pancréas, qui a lieu lorsque le taux de sucre dans le sang est important, ce qui permet de réguler la glycémie.
- Mastocytes : exocytose d’histamine essentiel à comprendre dans le phénomène d’allergie
Ch2 – Fig 34 : Les 2 types d’exocytose, constitutive et provoquée
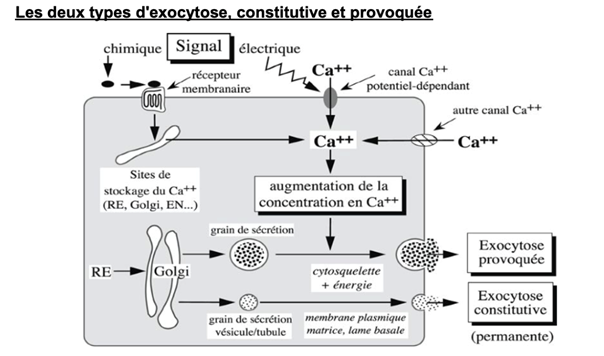
La fixation d’un ligand à un récepteur membranaire constitue un signal chimique, qui peut conduire à la libération de calcium depuis des sites de stockage.
Au niveau d’une jonction musculaire, la modification du potentiel de membrane correspond à une stimulation électrique qui provoque l’entrée de calcium dans la cellule.
Ainsi, l’augmentation de la concentration en calcium dans le cytosol est à l’origine d’une sécrétion, ou d’une exocytose.
EXEMPLE
- Les cellules bêta du pancréas libèrent de l’insuline pour réguler la glycémie. C’est un processus d’exocytose provoquée, qui a lieu à cause de l’augmentation du sucre dans le sang.
- Les mastocytes, un type de cellule immunitaire, utilisent l’exocytose pour libérer des substances comme l’histamine, la sérotonine et diverses enzymes, particulièrement en réponse à, des réactions allergiques.
Ch11 – Fig 21: Les 2 conformations, ouverte et fermée, du récepteur nicotinique de l’acétylcholine
L’entrée de calcium est ici dû à un potentiel électrique et conduit à une exocytose massive du neurotransmetteur.
- VI- Biosynthèse et renouvellement de la MP
- Ce renouvellement est permanent
En microscopie quantitative, on observe que le renouvellement de la membrane plasmique est permanent mais que sa vitesse varie selon la cellule :
- 100% de la membrane plasmique d’un fibroblaste est endocytée en 125 minutes (ou environ 2h)
- L’endocytose de toute la membrane plasmique d’un macrophage ne se fait qu’en 33 minutes.
Rappel : L’endocytose consiste à prélever une portion de la membrane plasmique pour former une vésicule tandis que pour l’exocytose la vésicule fusionne avec la membrane plasmique y ajoute un peu de son propre contenu
B. Les étapes
Ch2 – Fig 35 : Schéma général de la biosynthèse des constituants de la membrane plasmique
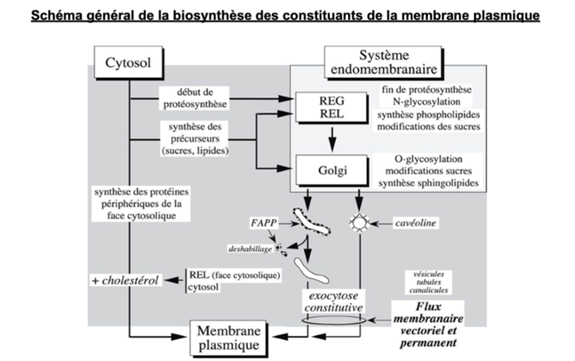
FAPP : Four-phosphate AdaPtor Protein
La très grande majorité des constituants de la membrane plasmique est apportée à partir du golgi par les tubules (recouvertes de FAPP puis déshabillés) les cavéoles n’apportent qu’une fraction minoritaire des constituants membranaires
- Au sein du réticulum endoplasmique lisse (REL), certaines protéines vont subir une glycosylation.
- Ensuite, les protéines passent par l’appareil de Golgi où elles subissent un autre type de glycosylation et d’autres modifications.
- Après le passage dans le Golgi, des vésicules se forment et sont acheminées vers la membrane par exocytose constitutive. Ces vésicules peuvent être recouvertes soit de cavéoline, soit des tubules qui émanent du Golgi, recouvert de FAPP qui se déshabille avant de fusionner avec la MP
→ Une partie des composés de la MP vient du SE et l’autre du cytosol
Se frome un flux membranaire vectoriel permanent (FMVP) lié à la sécrétion constitutive.
Ch8 – Fig 18 : Les 4 types de matériel membranaire exportés par le Golgi trans et le réseau transgolgien (TGN) selon leur destination et la nature de leur revêtement cytosolique
C. Les déchirures de la membrane plasmique
Les déchirures peuvent être causé par des facteurs externes (exogène).
La contraction musculaire peut entraîner des déchirures membranaires. Cependant, la dysferline est une protéine de la membrane plasmique impliquée dans la réparation de la membrane des cellules musculaires.
La mutation du gène codant pour la dysferline peut être à l’origine d’une dystrophie musculaire des ceintures, c’est-à-dire d’une maladie qui peut empêcher les mouvements (par exemple, une personne souffrant de cette pathologie ne peut plus marcher).
Dystrophie musculaire des ceintures :
- Lamine A/CCavéolineCalpaïneDysferlineSarcoglycan a, b, g, d
D. Les déformations de la membrane plasmique
Les déformations de la membrane plasmique permettent à la cellule :
- D’explorer son environnement et de se déplacer
- Communiquer avec d’autre cellule (important pour les cellules du systèmes immunitaire).
QUESTION REPONSE 2023
Question 1 : Quelle est la raison pour laquelle les cadhérines sont des protéines transmembranaires et ancrées ?
Réponse : Les cadhérines sont structurées de cette manière pour remplir leur fonction spécifique, qui est d’adhérer les cellules les unes aux autres au sein des tissus. Leur configuration transmembranaire leur permet de traverser la membrane et de se fixer solidement dans le cadre de leur rôle d’adhésion cellulaire.
Question 2 : Les protéines périphériques peuvent-elles interagir avec les parties extracellulaire et intracellulaire des protéines intégrales ?
Réponse : Oui, les protéines périphériques ont la capacité d’interagir avec les régions extracellulaires et intracellulaires des protéines transmembranaires. Elles peuvent se fixer sur la face interne de la membrane plasmique et peuvent être liées par des groupes acyle ou par des molécules lipidiques membranaires.
Question 3 : Où sont synthétisées les protéines intégrales ?
Réponse : Les protéines intégrales sont synthétisées dans le réticulum endoplasmique granuleux (REG) et migrent à travers le système endomembranaire, qui comprend le transport vers l’appareil de Golgi et éventuellement vers la membrane plasmique ou d’autres destinations cellulaires.
